動物衛生研究部門
IV.原子吸光法による臓器中 鉛の測定
測定原理
生体材料である肝臓や腎臓内の鉛を測定するためには試料に強酸を加え加熱、組織を灰化し、金属元素を組織から解離する。その後有機溶媒で鉛を抽出し、原子吸光分光光度計で測定する
参考文献
- 原田 章, 他:鉛 健康診断の進め方 全衛連, 62-63, 1990
目次
1.準備物
1.器具
- 原子吸光分光光度計(フレーム型)
- ケルダール分解装置
- ケルダールフラスコ (50 ml容)
- 分液ロート(100~200 ml容)
- ビーカー(100 ml容)
- 試験管バサミ
ガラス器具は酸洗浄済みのもの
-酸洗浄-
通常の洗浄は、1%硝酸に一晩浸けて乾燥させる
原子吸光分光光度計(定量演算機能付き)

ケルダール分解装置(水流ポンプ付き)

ケルダールフラスコ(50 ml容) 試験管バサミ、分液ロート
2.試薬
- 硝酸 (精密分析用)
- 硫酸 (精密分析用)
- 過塩素酸 (精密分析用)
- 鉛標準液 (原子吸光分析用)
- アンモニア水 (精密分析用)
- 塩酸ヒドロキシルアミン (原子吸光分析用)
- ピロリジンジチオカルバミン酸アンモニウム(APDC:原子吸光分析用)
- メチルイソブチルケトン(MIBK:原子吸光分析用)
2.試薬調製法
(1)標準液
鉛高濃度標準液
鉛標準液 1.0 ml に 1N 塩酸を加え全量を100 mlにする(表-1)
(表-1)
| 市販品 | 標準液 | 1N 塩酸 | 濃度 |
|---|---|---|---|
| 鉛標準液 (1000 mg/L) |
1.0 ml | 全量を100 mlにする | 鉛濃度は1000 μg/dl |
鉛測定用標準液
高濃度標準液を所定量取り、1N 塩酸で全量を10 mlにする(表-2)
(表-2)
| 標準液 | 高濃度標準液 (ml) |
1N 塩酸 (ml) |
全量(ml) | 最終鉛濃度(μg/dl) |
|---|---|---|---|---|
| Blank | 0.00 | 10.0 | 10.0 | 0 |
| Std 1 | 1.5 | 8.5 | 10.0 | 150 |
| Std 2 | 3.0 | 7.0 | 10.0 | 300 |
(2)試薬
- 過塩素酸:硫酸(4:1)混液
作製する混合液の倍以上のビーカーに、過塩素酸を静かに入れる。
次いで、ガラス棒を伝わせ硫酸を少量ずつ加える。
100 mlの混合液を作る場合は200~300 mlのビーカーを使用)
混合液は発熱するので注意 - 1N塩酸
濃塩酸を蒸留水で12倍する。
酸塩基試薬の調製法 - 10%塩酸ヒドロキシルアミン(使用時調整)
10 gを蒸留水で溶解し、総量を100 mlにする(一検体5 ml使用) - 2%ピロリジンジチオカルバミン酸アンモニウム(使用時調整)
2 gを蒸留水で溶解し、総量を100 mlにする(一検体10 ml使用)
3.操作手順
(1)サンプル秤量
サンプル10 gをケルダールフラスコに入れる。
調整した鉛測定用標準液をケルダールフラスコに10 ml入れる
(鉛として0 μg、15 μg、30 μg)
(2)硝酸を20 ml加える。
(3)ケルダール分解装置で加熱分解。
60~90分後、液量が2~3 ml位になったら、装置からおろして放冷する。
試料を入れる 左:ブランク 右:肝臓(10 g)
硝酸20 ml添加 左:ブランク 右:肝臓
加熱開始約10分後泡が出始める 左右:肝臓
開始約15分後泡がたくさん出る 左右:肝臓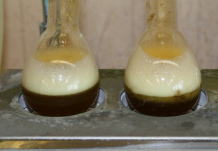
開始約20分後右側は泡の出が少なくなる 左右:肝臓
開始約30分後液が褐色になる 左右:肝臓
開始約45分後液の色が薄くなる 左右:肝臓
開始約60~90分後液量が少なくなる(約3 ml) 左右:肝臓
冷えると液は黄色透明 左:ブランク 右:肝臓
(4)過塩素酸:硫酸(4:1)混液を10 ml加えて、再びケルダール分解装置で加熱分解。
2~3時間後、泡が出なくなり、液量が2~3 ml、無色から薄い黄色、透明になれば分解終了、放冷する。
混液を加え分解開始 左:ブランク 右:肝臓
混液が温まり試料から泡が出てくる 左:ブランク 右:肝臓
ブランクからも泡が出る、黄色に変化 左:ブランク 右:肝臓
液が黄色に変化し、白煙が出る 左:ブランク 右:肝臓
液が少なくなりブランクは無色透明、肝臓は淡黄色透明 左:ブランク 右:肝臓
冷えるとブランク、肝臓とも無色透明になる 左:ブランク 右:肝臓
(5)灰化液を100 ml 容のビーカーに入れる。フラスコに蒸留水を入れよく洗い、洗液もビーカーに入れ約50 mlにする
(6)10%塩酸ヒドロキシルアミン5 mlを加え、小型の攪拌子をビーカーに入れ攪拌する
攪拌子は入れたまま
(7)ビーカーをpHメーターにセットする
ビーカーの下にはスターラーをセットする
pHメーターの電極に必ず電極保護カバーをつける
(8)アンモニア水でpHを3.5にする
pH微調整のためアンモニア水、硝酸の10倍希釈液、100倍希釈液を作ると便利。
(9)pHを調整した液を分液ロートに入れる。
(10) 2%ピロリジンジチオカルバミン酸アンモニウム(APDC)を10 ml加え30秒位よく振る
(11)メチルイソブチルケトン(MIBK)を2 ml加え5分間振盪する。
(12)数分間放置し、MIBK層を試験管に入れ、原子吸光分光光度計で283.3 nmの吸収波長を測定する
灰化液とフラスコを共洗いした液約 50 ml 左:ブランク 右:肝臓
アンモニア水でpHを3.5にする 
分液ロートに入れる 左:ブランク 右:肝臓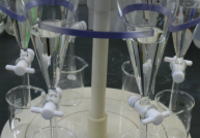
2%APDCを10 ml加えた直後 左:ブランク 右:肝臓
APDCを加えよく振った後 左:ブランク 右:肝臓
液面の状態 肝臓
MIBKを加え5分間振盪後 左:ブランク 右:肝臓
上層(黒色)がMIBK 肝臓
MIBK層 左:ブランク 右:肝臓
4.補足説明
(1)検量線
標準液(0、15、30 μg)を測定し検量線を作成する。
(2)試料濃度
作成した検量線から試料の鉛量を求める。
例)
求めた値が25 μg、使用した試料が10 gであれば、試料の鉛量は25 μg/10 g (2.5 μg/g=2.5 ppm)
(3)正常牛、中毒牛の鉛量(ホルマリン固定材料)
参考:上原 修一、他:子牛の鉛中毒 日獣会誌、41 822-824、1988
正常子牛
- 肝臓Pb 1.0~3.0 ppm
- 腎臓Pb 1.0~5.0 ppm
鉛中毒子牛
- 肝臓Pb 2.5~14.1 ppm
- 腎臓Pb 6.2~44.3 ppm

